رتبت العناصر في الجدول الدوري بناء على كتلها الذريه
جدول المحتويات
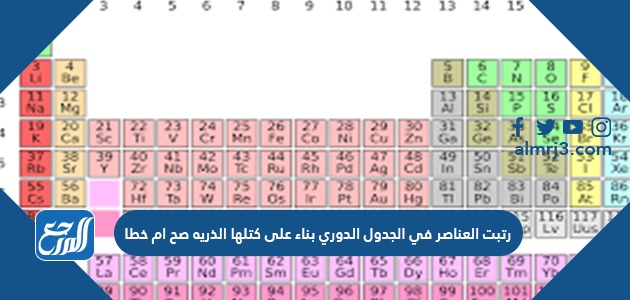
رتبت العناصر في الجدول الدوري بناء على كتلها الذريه صح ام خطا؟ الجدول الدوري هو عبارة عن ترتيب العناصر الكيميائية، فالعناصر التي لها نفس السلوكيات الكيميائية يتم وضعها في نفس العمود، ويطلق على الصفوف اسم الدورات، أما الأعمد يطلق عليها مجموعات، لذا ومن خلال موقع المرجع سوف نعرض إليكم رتبت العناصر في الجدول الدوري بناء على كتلها الذريه صح ام خطا في السطور التالية.
الجدول الدوري
هو عبارة عن ترتيب العناصر الكيميائية في جدول، تم ترتيبها وفقًا للعدد الذري، والخواص الكيميائية المتكررة، والتوزيع الإلكتروني، العناصر في الدورة الواحدة تتكون من لافلزات على اليمين، وفلزات على اليسار، والعناصر التي لها السوك نفسها يتم وضعها في العمود نفسه، تسمى الصفوف بالدورات أما الأعمدة تسمى بالمجموعات، وكل ستة مجموعات لها أسماء وارقام مخصصة، أول من قام بنشر الجدول الدوري هو العالم ديمتري مندلييف عام 1869م، ومن ثم تم تطويره من أجل توضيح الاتجاهات الدورية للعناصر المعروفة، وتم تطوير الجدول الدوري حتى أصبح على ما هو عليه الآن، حيث يمتلك إطار مفيد من أجل تحليل التفاعلات الكيميائية، ويتم استخدامه في الكيمياء والفيزياء النووية وفي عدة مجالات علمية أخرى، تم تركيب العناصر من العدد الذري 1 حتى 118، يوجد 98 عنصر في الطبيعة، فبعضها يوجد بكميات قليلة، والبعض الآخر تم تصنيعه في المختبرات قبل العثور عليه في الطبيعة. [1]
اقرأ أيضًا: بالرغم من أن العالمين مندليف، و ماير إلا أنه اقترن اسم العالم مندليف بالجدول الدوري؛ وذلك بسبب
رتبت العناصر في الجدول الدوري بناء على كتلها الذريه صح ام خطا
يتم ترتيب العناصر الكيميائية في الجدول الدوري وفقًا للتوزيع الإلكتروني، والعدد الذري والخواص الكيميائية التي تتشابه مع بعضها البعض، حيث يحتوي الجدول الدوري على 7 دورات و18 عمود، ورقم كل دورة يشير إلى عدد الإلكترونات التي توجد في مستويات طاقتها، والإجابة عن سؤال رتبت العناصر في الجدول الدوري بناء على كتلها الذريه صح ام خطا يكون كالتالي:
- العبارة صحيحة.
خصائص الجدول الدوري
يتم استخدام الجدول الدوري في العديد من الاستخدامات المختلفة كالكيمياء والفيزياء النووية وغيرها من الاستخدامات العلمية المتنوعة، ومن أبرز خصائص الجدول الدوري:
- الجدول الدوري عبارة عن 7 دورات أفقية، و18 مجموعة رأسية.
- تبدأ المجموعات الرأسية به من جهة اليسار وتنتهي من اليمين.
- تنفصل المجموعة 2A عن المجموعة 3A بدءً من الدورة الرابعة بمجموعة العناصر الإنتقالية.
- ترتيب العناصر يكون بناءً على أعدادها الذرية، وكل دورة تبدأ بعد أن يمتلىء كل مستوى طاقة.
- رقم الدورة الواحدة يدل على عدد مستويات الطاقة لذرة العنصر.
- رقم المجموعة يدل على عدد الإلكترونات التي توجد في مستوى الطاقة الأخير للذرة.
- كل مجموعة رأسية تحتوي على مجموعة من العناصر المتشابهة في خواصها الكيميائية.
- في أقصى اليمين يوجد مجموعة صفرية تحتوي على الغازات النبيلة يرمز لها ب o.
أهمية الجدول الدوري
بعد أن ذكرنا لكم الإجابة عن سؤال ترتيب العناصر في الجدول الدوري يكون بناءً على الكتلة الذرية سوف نعرض أهمية الجدول الدوري، حيث يحتوي الجدول الدوري على 118 عنصر ذري، لكل عنصر منهم استخدام خاص به، ويكمن أهمية الجدول الدوري في التالي:
- التعرف على البنية الإلكترونية لذرة العنصر.
- معرفة التفاعلات الكيميائية التي يمكن أن يدخل العنصر فيها.
- التعرف على سلوك العنصر الكيميائي.
- تحديد موقع العنصر سواء في المجموعة أو الدورة.
اقرأ أيضًا: أغلب العناصر الموجودة على يسار الجدول الدوري هي
ذكرنا لكم في ذا الموضوع رتبت العناصر في الجدول الدوري بناء على كتلها الذريه صح ام خطا؟، بالإضافة إلى معرفة ما هو الجدول الدوري، و الاستخدامات المختلفة للجدول الدوري، بالإضافة إلى ذكر أهمية الجدول الدوري، حيث يدخل في العديد من الاستخدامات المختلفة.
المراجع
- wikiwand.com , الجدول الدوري , 15/09/2021