تتكون الروابط التساهمية عندما

جدول المحتويات
تتكون الروابط التساهمية عندما، الكيمياء من أحد أهم العلوم الموجودة في العالم، الكيمياء هي أساس صناعة الدواء وصناعة الأسلحة النووية والتي تُعتبر أكثر الصناعات المهمة التي ترتكز عليها كل دولة، كما أن مواضيع الكيمياء كثيرة لذلك سيتناول موقع المرجع كافة المعلومات حول الرابطة التساهمية ومكونات الروابط التساهمية.
ما هي الرابطة التساهمية
الرابطة التساهمية هي رابطة كيميائية تتكون بين الذرات من خلال مشاركة الإلكترونات،و هي تشارك الذرات بالإلكترونات عن طريق جذبها إلى أنويتها، تحتوي الروابط التساهمية على مواد غير عضوية مثل: الهيدروجين والكلور والنيتروجين والماء والأمونيا مع جميع مركبات عضوية، تتميز الروابط التساهمية بأنها من أقوى الروابط التي تربط بين الذرات وبعضه، كما إنها تتشكل عندما تكون الطاقة الإجمالية للذرات المترابطة أقل من الموجودة في الذرات المتفرقة.[1]
اقرأ أيضًا: تقرير عن سير العمل في المدرسة
تتكون الروابط التساهمية عندما
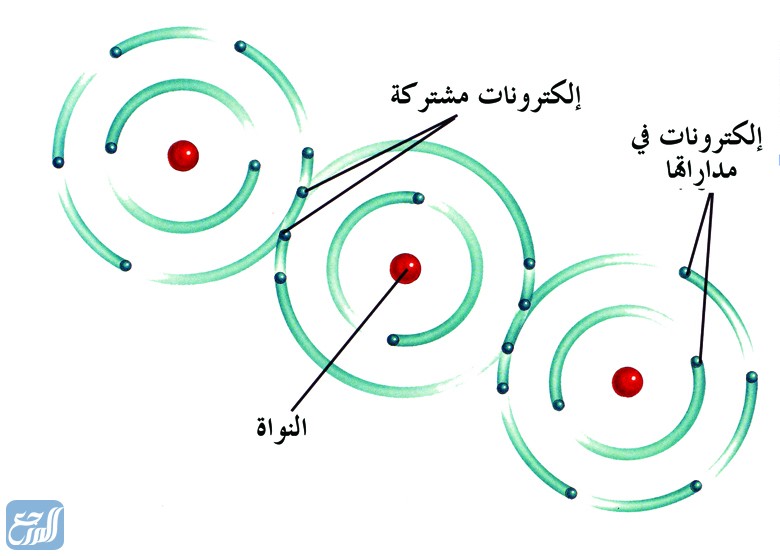
الرابطة التساهمية هي أحد أشكال الترابط الكيميائي وتتميز بمساهمة زوج أو أكثر في الإلكترونات بين الذرات مما ينتج عنه تجاذب جانبي يعمل على تماسك الجزء الناتج وتميل الذرات للمشاهمة أو المشاركة بإلكتروناتها بالطريقة التي تجعل غلافها الإلكتروني ممتلئ وهذه الرابطة دائماً أقوى من القوى بين الجزيئات، وتتحدث غالبا بين الذرات التي لها سالبية كهربية عالية، والإجابة الصحيحة هي:
- تتكون الرابطة التساهمية عندما تشترك زوج أو أكـثر من الإلكترونات بين ذرتين.
اقرأ ايضاً: ما هو اول عنصر في الجدول الدوري.
ما الشروط اللازمة لحدوث الرابطة التساهمية؟
لحدوث الرابطة التساهمية شروط منها ما يختصّ بعدد إلكترونات المدار الأخير للذرات، ومنها ما يكون له علاقة بالكهروسلبية والميل لتشارك الإلكترونات ومنها ما يهتم بالقوى الإلكتروستاتيكية والجذب بين الأنوية والإلكترونات:[1]
- كل ذرة من الذرات المترابطة تحتوي على 5 إلكترونات في مدار التكافؤ على الأقل أي يُسمح بامتلاكها 6 أو 7 إلكترونات أيضًا، وبذلك تحتاج الذرات إما إلى مشاركة 3 إلكترونات للوصول إلى 8 (اكتمال مدار التكافؤ الخارجي وتستقرّ) أو إلكترونين أو إلكترون واحد.
- يكون فرق الكهروسلبية بين الذرات قليل جدًا حيث لا يكفي لانتقال إلكترونات وتكوين أيونات فيتم تشكيل رابطة تساهمية من خلال مشاركة الإلكترونات فتكون الذرات أكثر ميلًا لمشاركة الإلكترونات من الفقد والكسب.
- كل نواة تجذب الإلكترونات المشتركة بنفس المقدار، ولولا ذلك لما نتج استقرار وتوازن بين ذرات التي تتشارك في الإلكترونات.
ما هي خصائص الرابطة التساهمية؟
تعرف الرابطة التساهمية بمجموعة من الخصائص التي تميّزها، ومن خصائص الرابطة التساهمية ما يأتي:
- نقاط الغليان والانصهار تكون عند درجات حرارة منخفضة: وذلك بسبب ضعف قوى الجذب وإمكانية التغلّب دون الحاجة إلى طاقة كبيرة، ولذلك يلاحظ بأن أغلب المركبات التي ترتبط بهذه الرابطة تكون بالحالة السائلة وحتى الغازية عند درجة حرارة عادية كدرجة حرارة الغرفة.
- من السهل تعرّض الجزيئات الصلبة التي ترتبط بالروابط التساهمية للكسر: سهولة الكسر ناجمة عن ضعف قوة الروابط التساهمية ومرونتها أو هشاشتها.
- موصلات سيئة للكهرباء والحرارة: على عكس المركبات الأيونيّة والمعادن، فإن الجزيئات هنا لا تقوم بإيصال التيار الكهربائي أو الحرارة بكفاءة.
- المحتوى الحراري اللازم للتبخر أو الذوبان منخفض: يعبّر هذا المحتوى عن كمية الطاقة التي نحتاجها لتبخير مول واحد من المادة السائلة أو إذابة مول واحد من المادة في الحالة الصلبة بشرط ثبات الضغط ويكون هذا المحتوى قليل في الرابطة التساهمية.
- المركبات قابلة للاشتعال: العديد من المركبات تتكوّن من الهيدروجين والكربون (مركبّات عضوية)، وذلك بسبب تشابههم في الكهروسلبية، وهذه المكونات هي ما تجعل المركبّات قابلة للاشتعال عند تفاعلها مع الأكسجين واحتراقها.
اقرأ أيضاً: حل كتاب العلوم ثالث متوسط ف1 الفصل الاول.
إلى كم نوع تنقسم الرابطة التساهمية؟
تتكوّن الرابطة التساهمية عن طريق مشاركة زوج أو أكثر من الإلكترونات عن طريق جذب أنوية الذرات الموجبة للإلكترونات السالبة وتنقسم الرابطة التساهمية إلى عدة أقسام بناءً على معيارين أساسيين، أحدهما عدد الأزواج المشتركة والآخر يعتمد على فرق الكهربية،وفيما يأتي هذه الأنواع:
اعتمادًا على أزواج الإلكترونات المشتركة يمكن أن تتشارك الذرات بزوج من الإلكترونات أو أكثر ومن أنواع الرابطة التساهمية بناءً على ذلك:
- الرابطة التساهمية الأحادية هي الرابطة التي تتكوّن من تشارك زوج إلكترونات واحد بين الذرتين المرتبطتين، ومن الأمثلة على ذلك: كلوريد الهيدروجين ورمزه الكيميائي HCl، جزيء الهيدروجين ورمزه الكيميائي H2.
- الرابطة التساهمية الثنائية الرابطة التساهمية الثنائية هي الرابطة التي تتكوّن من تشارك زوجين من الإلكترونات بين الذرتين المرتبطتين، ومن الأمثلة على ذلك: ثاني أكسيد الكربون ورمزه الكيميائي CO2، غاز الأكسجين ورمزه الكيميائي O2.
- الرابطة التساهمية الثلاثية الرابطة التساهمية الثلاثية، هي الرابطة التي تتكوّن من تشارك ثلاثة أزواج من الإلكترونات بين الذرتين المرتبطتين، ومن الأمثلة على ذلك: النيتروجين ورمزه الكيميائي N2.الأسيتيلين ورمزه الكيميائي C2H2.
لقد وصلنا إلى نهاية مقالتنا العلمية حول تتكون الروابط التساهمية عندما، حيث تطرقنا إلى الروابط التساهمية وخصائصها وأهم الشروط اللازمة لحدوثها.
المراجع
- britannica.com , Covalent bond , 05/09/2021