الانتروبي هو عبارة عن
جدول المحتويات
الانتروبي هو عبارة عن؟ هو سؤال يتردد في أذهان الباحثين والدارسين في مجال الفيزياء والكيمياء؛ حيث أن هذا المبدأ يُعد من المبادئ المهمة التي يمكن تطبيقها في العديد من مجالات الحياة، لذلك يقدم موقع المرجع تعريف مبدأ الانتروبي، ومن هو مؤسسه، وإستخداماته، وأهميته في حياتنا، وبعض الأمثلة عن الانتروبي.
الانتروبي هو عبارة عن
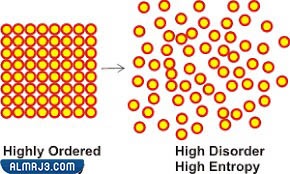
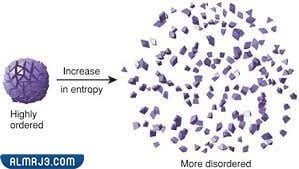
الانتروبي هو عبارة عن القصور الحراري، ويُطلق عليه بالإنجليزية اسم الانتروبيا، وهو عبارة عن مقياس تم استخدامه لمعرفة نسبة عشوائية واضطراب النظام الديناميكي الحراري، أي أن قيمته تتغير بتغير كمية المواد الموجودة. تُقاس الانتروبي بإستخدام وحدة جول لكل وحدة كلفينية J/K.
ما هو الانتروبي
عرف علماء الفيزياء والكيمياء الانتروبي أو الانتروبيا وفقًا للقانون الثاني في الترموديناميك على أنها القصور الذاتي الحراري، وهو عبارة عن مقياس يُستخدم في قياس نسبة ميل أي نظام مغلق إلى عملية التحول التلقائي بهدف الوصول إلى حالة تُسمى بحالة التوزيع المتساوي داخل جميع الأجزاء مثل الكثافة المتساوية أو الضغط المتساوي أو درجات الحرارة المتساوية.[1]
شاهد أيضًا: اذا اثرت قوة في جسم متحرك وزادت سرعته
من هو مؤسس مبدأ الانتروبي
عالم الفيزياء الألماني رودولف كلوسيوس هو مؤسس مبدأ الانتروبي، وقد قدم هذا العالم فرضية قانون الديناميكا الحرارية الثاني في عام 1950م للتأكيد على هذا المبدأ من خلال تطبيق هذه الفرضية، والتي نصت على عدم إمكانية انتقال الحرارة من جسم ذي حرارة باردة إلى جسم ذو حرارة مرتفعة، مع التأكيد على أن مبدأ الانتروبي يعني عملية تبديد الحرارة الموجودة.
متى يقل الانتروبي
تتغير قيمة الانتروبي بتغير كمية المادة أي أنه كلما زاد اضطراب المادة في الوسط، وزاد انتشار جزيئاتها في اتجاهات مختلفة؛ زاد الانتروبي، بينما يقل الانتروبي عند يصبح النظام مرتبًا، ويقل اضطراب المادة وانتشار جزيئاتها في الوسط. ويُشار إلى الانتروبي بإستخدام الرمز S.
شاهد أيضًا: قابلية المادة للانسياب والانتشار تسمى
وحدة قياس الانتروبي
إن الانتروبي أو الانتروبيا هي أداة أو مقياس يُستخدم في قياس قيمة عشوائية المادة أو الفوضى الموجودة في أي نظام. يُقاس الانتروبي بإستخدام وحدة قياس جول/ كلفن. كذلك نجد أن الانتروبي له خاصية وهي أنه إما يكون سالبًا أو موجبًا وفقًا للديناميكية الحرارية.
أمثلة عن الانتروبي
يوجد الكثير من الأمثلة عن الانتروبي، ومن أهم هذه الأمثلة ما يلي:
- عملية ذوبان مكعب من الثلج؛ حيث إنه عند حدوث هذا الذوبان؛ يزداد الانتروبي نتيجة انتشار جزيئات المادة في الوسط، وحدوث فوضى داخل النظام نتيجة حدوث ذلك.
- عند تحول السائل من الحالة السائلة إلى الحالة الغازية؛ حيث أن طاقة النظام تزداد بزيادة نسبة تبخر الماء عند تحوله من كونه سائل إلى غاز، كما أن مع ازدياد عملية التحول؛ نلاحظ زيادة نسبة الفوضى، ومن ثَم زيادة الانتروبي.
- الشمس والقمر؛ حيث أن الشمس حجمها كبير أي أن هناك إمكانية لحركة جزيئاتها وعدم انتظامها، مما يؤدي إلى ارتفاع درجة الحرارة، ومن ثَم زيادة الانتروبي. أما بالنسبة للقمر؛ فنجد أنه يحتوي على عدد قليل من الجزيئات، مما يؤدي إلى جعل درجة الحرارة باردة عليه.
أهمية الانتروبي في حياتنا
لقد أشارت نتائج الأبحاث والدراسات التي تمت خلال السنوات الماضية إلى أن مبدأ الانتروبي قد ساهم في تطوير علم الكيمياء الحيوية من خلال دراسة اتحاد الخلايا الحية مع بعضها بشكل منتظم؛ ذلك الأمر الذي ساعد في اكتشاف كيفية إنتاج الأعضاء الصناعية والأنسجة بالاعتماد على أسس الديناميكا الحرارية.
من جانب أخر؛ نجد أنه تم استخدام مبدأ الانتروبي كفرضية للتعرف على سبب مُضي الوقت إلى الأمام، مع عدم وجود إمكانية لعكسه، لذلك سيكون لدينا دائمًا في هذا الكون ماضي ومستقبل من خلال تطبيق هذا المبدأ في حياتنا.
وبذلك نكون قد توصلنا إلى أن الانتروبي هو عبارة عن القصور الحراري، وهو أحد مبادئ علم الفيزياء والكيمياء الذي تم استخدامه بشكل كبير في حياتنا، وقد نتج عنه العديد من الاكتشافات في مجالات مختلفة.
المراجع
- britannica.com , entropy , 26/09/2021