فئة العنصر الذي توزيع إلكترونات تكافئه s2d1هو
جدول المحتويات
فئة العنصر الذي توزيع إلكترونات تكافئه s2d1هو، يمتلك كل عنصر بالجدول الدوري خصائص فريدة له وتوزيع الكتروني بحسب العدد الذري له، ومن خلال موقع المرجع سنُجيب عن السؤال العلمي المطروح أعلاه، بالإضافة إلى التطرق لبعض التعريفات والمصطلحات في علم الكيمياء، كتعريف العنصر وأنواعه، والجدول الدوري والإلكترونيات.
ما المقصود بالعنصر
يشير مفهوم العنصر إلى المادة التي تحتوي على نوع ذرة خاص فيها، ولها خصائصها، ولا يمكن تقسيمها إلى أي مادة أخرى، في الكون يحتوي كل شيء على ذرات عنصر واحد أو أكثر على الأقل، وبلغ مجموع العناصر الموجودة في الكون حوالي 100 عنصر، حيث يقوم الجدول الدوري بسرد جميع العناصر المعروفة في الكون، ويجمع العناصر ذات الخصائص المتشابهة معًا. [1]
ما أنواع العناصر
يتم تقسيم العناصر حسب الحالة صلبة أو سائلة أو غازية، وإن كانت مادة مُوصلة للكهرباء و الحرارة أو مادة عازلة، ومن هذه الأنواع التي يختلف كل نوع فيها عن الأخرى وفق خصائصها و صفاتها:[2]
- فلزات(معادن): غالبية العناصر الموجودة في الجدول الدوري هي الفلزات أو المعادن،ويتم تقسيم المعادن بواسطة اللافلزات من خلال خط متعرج يبدأ من الكربون، وينتهي حتى عنصر الرادون،كذلك توجد بينهما العناصر هي الفوسفور والسيلينيوم واليود، ويتضمن ذلك الفلزات القلوية، والمعادن الانتقالية، واللانثانيدات، والأكتينيدات، والمعادن الأرضية القلوية.
- أشباه فلزات: هي العناصر الموجودة على يسار الخط في الجدول الدوري، وتُسمى شبه معدنية أو أشباه فلزات، و تكون لهذه العناصر مزيج من الخصائص الموجودة لكل من المعادن واللافلزات.
- لافلزات: تكون موجودة في الجزء الأيمن من الجدول الدوري، و تتسم بخصائص فيزيائية و كيمائية تُمكن من التفريق بينها و بين الفلزات، بأنها ليست لامعة أو يمكن تشكيلها، كذلك أنها ليست مُوصلة جيدة للكهرباء و الحرارة.
شاهد أيضًا: أكبر عنصرين شيوعا في الكون
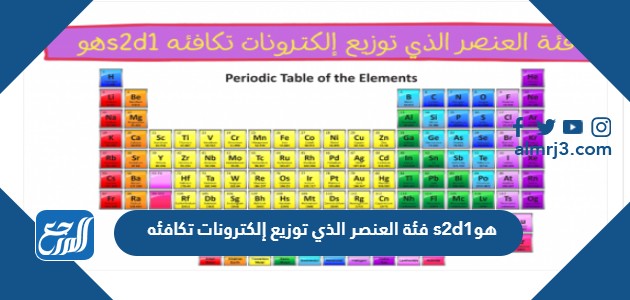
فئة العنصر الذي توزيع إلكترونات تكافئه s2d1هو
تقوم الإلكترونات بالدوران حول نواة الذرة في مدارات أو مستويات أو مجالات الطاقة، حيث مجال الطاقة الأقرب للنواة وهو المجال الأول يتسع فقط لإلكترونين، ومجال الطاقة الثاني يتسع لثمانية إلكترونات، ومجال الطاقة الثالث يمكن أن تتسع وتستوعب ما يصل إلى ثمانية عشر إلكترون، ويتم تحديد فئة العنصر من خلال المجال الأخير في الطاقة، و التوزيع الإلكتروني الخاص فيه، ومن هذا المنطلق نجد أن الإجابة هي:
- العنصر Mg12، حيث أن توزيعه الإلكتروني [Ne], 3S2 ، ضمن الدورة الثالثة و المجموعة 2A.
- العنصر Ge32، حيث أن توزيعه الإلكتروني,[Ar] ,4S2 ,3D10 ,4P2 ضمن الدورة الرابعة و المجموعة 4A.
شاهد أيضًا: يسمى اصغر جزء في العنصر
ما المقصود بالإلكترونيات
طور العالم الدنماركي نيلز بور نموذج الذرة في عام 1913، حيث قام بإظهار الذرة كنواة مركزية تحتوي على البروتونات والنيوترونات بالإضافة إلى الإلكترونات، ومُحاطة بأغلفة إلكترونية في أغلفة إلكترونية دائرية على مسافات محددة من النواة، حيث أن لكل غلاف إلكتروني مستوى طاقة مختلف، فيتسع المستوى الأول من الطاقة لعدد قليل من الإلكترونات، وكلما ابتعدت مستويات الطاقة اتسعت لعدد أكبر من الإلكترونات.
ما هو الجدول الدوري
المراجع
- bbc.co.uk , What are elements? , 11/9/2021
- byjus.com , Chemistry Metals and Nonmetals , 11/9/2021
- khanacademy.org , The periodic table, electron shells, and orbitals , 11/9/2021








