كيف اعرف اذا المركب قطبي او غير قطبي
جدول المحتويات
كيف اعرف اذا المركب قطبي او غير قطبي، علم الكيمياء هو العلم الّذي يتم فيه تشكيل غالبية المركبات والمواد الّتي نستخدمها بشكلٍ يومي، وتتشكل هذه المواد عن طريق مجموعة من التفاعلات والروابط الّتي تنشأ بين العناصر المختلفة، وسيقدّم لنا موقع المرجع في هذا المقال شرحاً موسعاً عن إحدى هذه الروابط وهي الرابطة التساهمية وما هو الفرق بينها وبين الرابطة الأيونية، وكذلك سوف يجيبنا على سؤالنا بطريقة سهلة وواضحة.
ما هي الرابطة التساهمية
هي الرابطة الّتي تنشأ بين الجزيئات المتشابهة في الكهروسلبية لكي تصل إلى الاستقرار، وهذا التشابه في الجزيئات يأتي من كونها تحتاج إلى نفس العدد من الإلكترونات في مدارها الأخير لكي تصل إلى استقرارها، وفي حال لم يمتلئ المدار الأخير تبقى الجزيئات في حالة عدم استقرار، وتسمّى الإلكترونات الّتي تملئ المدار الأخير إلكترونات التكافؤ.
شاهد أيضًا: الروابط القطبية تتشارك بالإلكترونات بالتساوي
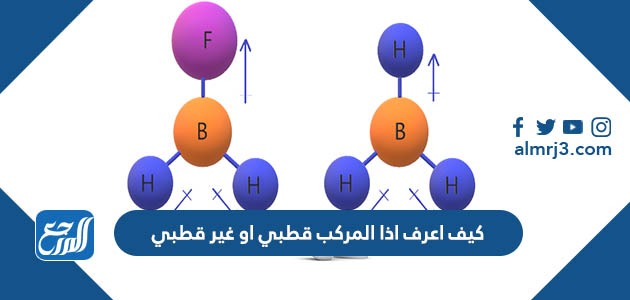
كيف اعرف اذا المركب قطبي او غير قطبي
من الممكن تمييز المركبات القطبية عن غير القطبية من خلال معرفة الكهروسلبية المتواجدة بين المركبين، حيث أنّ المركب الغير قطبي يكون له نفس التوزيع الإلكتروني بسبب التشابه في الكهرسلبية بين الذرات المكونة له وبالتّالي لا يكون له شحنة، أمّا المركب القطبي يحتوي على كهروسلبية مختلفة بين ذراته، وقد تكون هذه الكهرسلبية موجبة الشحنة؛ لأنّ الذرة الموجبة تكون هي الأقوى، وقد تكون سالبة نتيجة قوّة الذرة السالبة.[1]
شاهد أيضًا: تسمى الرابطة الناتجة عن تشارك الذرات بالإلكترونات رابطة ………………………
ما هي أنواع الرابطة التساهمية؟
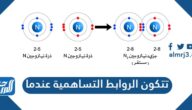
قد تتشكّل الرابطة التساهمية من اتحاد جزيئين لعنصر واحد مثل اتحاد جزيئين من الهيدروجين، وقد تتشكل من اتحاد جزيئين من عنصرين مختلفين، وبالتّالي فإنّ للرابطة التساهمية نوعين مختلفين هما:
الرابطة التساهمية القطبية
هي الرابطة المتشكلة بين جزيئين لهما كهروسلبية مختلفة بحيث يكون أحد الجزيئين ذو كهروسلبية مرتفعة بإمكانه أن يجذب الإلكترونات أكثر من الجزيء الآخر، وبالتّالي تتشكل هذه الرابطة، ولكن تكون الإلكترونات أقرب إلى أحد الجزيئين أكثر من الآخر.
الرابطة التساهمية الغير قطبية
وهي الرابطة الّتي تنشأ من اتحاد جزيئين لهما كهروسلبية متشابهة وغالباً يكونان من نفس العنصر، وفي حال كانا من عنصرين مختلفين يكون الفرق في الكهرسلبية بينهما لا يتجاوز 0.4، وتسمى هذه الرابطة بالرابطة النقية.
شاهد أيضًا: تبين الصيغ الكيميائية نوع الروابط وعددها في الجزئ
ما هي انواع الرابطة التساهمية عند تشكلها؟
قد يكون هنالك اختلاف في عدد الإلكترونات الّتي يحدث تشاركها بين الذرات عند تشكّل الرابطة التساهمية، وبحسب هذا الاختلاف نلاحظ وجود ثلاثة أنواع من الراوبط هي:
- الرابطة الأحادية: تنشأ من تشارك كل ذرة بإلكترون واحد فقط مثل الرابطة بين ذرّات الهيدروجين.
- الرابطة الثنائية: هي الرابطة الّتي تتشارك بها الذرات بإلكترونين مثل الرابطة بين ذرّات غاز ثنائي أكسيد الكربون.
- الرابطة الثلاثية: وهي الرابطة الّتي يتم فيها تشارك كل ذرة بثلاثة أزواج من الإلكترونات مثل الرابطة بين ذرّات غاز النيتروجين.
شاهد أيضًا: النقاط المحيطة برمز العنصر في التمثيل النقطي للإلكترونات تمثل
ما هي أهمية تمييز المركب القطبي عن الغير قطبي؟
إنّ تمييز المركب القطبي عن الغير قطبي له أهمية كبيرة في تحديد نوع المذيب الّذي يجب استخدامه مع المركبات، حيث أنّ المركبات القطبية لا يمكنها أن تذوب إلّا باستخدام المذيبات القطبية، بينما المركبات الغير قطبية لا تذوب إلّا في استخدام المذيبات الغير قطبية، ومن الجدير بالذكر بأنّ بعض المركبات يمكنها أن تذوب باستخدام المذيبات القطبية أو غير القطبية.
شاهد أيضًا: خريطة مفاهيم الروابط الكيميائية
ما نوع الروابط في الماء؟
ترتبط العناصر ضمن جزيء الماء من خلال روابط تساهمية تنشأ بين ذرات الهيدروجين وذرة الأوكسجين، حيث أنّ كل ذرة هيدروجين تحتاج إلى إلكترون في مدارها الخارجي لكي تحصل على الاستقرار الكيميائي، كما أنّ ذرة الأوكسجين تحتاج إلى إلكترونين لتثبت إلكترونياً، وبسبب ذلك يكون جزيء الماء مكوناً من ذرتي هيدروجين ترتبطان مع ذرة اوكسجين، فيصبح المدار الخارجي لكل منهما مستقراً كيميائياً، وبالتّالي فإنّ الماء يعتبر أحد المركبات القطبية.
شاهد أيضًا: الجسيمات المسؤوله عن تكوين الروابط هي
ما هي خصائص المركبات التساهمية؟
يوجد العديد من الخصائص الّتي تميز المركبات التساهمية عن غيرها، ومن أهم هذه الخصائص ما يلي:[2]
- هذه المركبات تعتبر ضعيفة في نقلها للتيار الكهربائي.
- من الممكن أن توجد هذه المركبات في الحالة الغازية أو الصلبة أو السائلة.
- المركبات في الحالة الغازية توجد في درجة حرارة الغرفة العادية وفي الضغط العادي.
- تمتلك المركبات الصلبة والسائلة عتبة حرارية منخفضة عند غليانها أو انصهارها.
- تمتلك هذه المركبات طاقة شبكية ضعيفة؛ لأنّ القوى المتواجدة بين الجزيئات تكون ضعيفة.
شاهد أيضًا: أي مما يأتي لايؤثر في سرعة التفاعل ؟
الفرق بين الرابطة التساهمية والايونية
تختلف الرابطة الأيونية عن الرابطة التساهمية في طريقة تشكّلها حيث تنشأ نتيجة فقد النواة إلكتروناتها لكي تصل إلى حالة الاستقرار الكيميائي في مدارها الأخير وبالتّالي فهي تكون متشابهة مع الغازات النبيلة، وتصبح الذرة الفاقدة للإلكترون موجبة الشحنة بسبب احتوائها على عدد من البروتونات يكون أكبر من عدد الإلكترونات، ويصبح اسم هذه الذرة فلز، والذرة الّتي تأخذ الإلكترونات تصبح سالبة الشحنة بسبب احتوائها على عدد من الإلكترونات أكبر من عدد البروتونات ويصبح اسمها لافلزات، أما الرابطة التساهمية فتنشأ نتيجة تشارك الذرات للإلكترونات بحيث تصل جميعها إلى حالة الاستقرار دون أي فقد في الإلكترونات.
وفي نهاية هذا المقال نكون قد أجبنا على سؤالنا كيف اعرف اذا المركب قطبي او غير قطبي، وكذلك تعرّفنا على ما هي الرابطة التساهمية، وما هي أنواعها وما هو الفرق بين هذه الأنواع، وكذلك شرحنا عن ما هي الأهمية في التمييز بين المركبات القطبية وغير القطبية.
المراجع
- chem.libretexts.org , 4.12: Shapes and Properties- Polar and Nonpolar Molecules , 14/08/2022
- byjus.com , Covalent Bond , 14/08/2022