العناصر في الجدول الدوري تترتب حسب اعدادها الكتلية
جدول المحتويات
العناصر في الجدول الدوري تترتب حسب اعدادها الكتلية؟، يعد هذا السؤال واحداً من الأسئلة المعروفة في علم الكيمياء والمطروحة في الكتاب المدرسي، ومن الواضح أهمية الطلاب في البحث عن إجابة مختصرة لهذا السؤال، كما أنّه من أحد المواضيع العلمية المطروحة ضمن المناهج التدريسية، والتي تركز على إحاطة الطالب علماً بالمقصود بالعناصر وأهميّة الجدول الدوري في دراسة الكيمياء، وانطلاقًا من هنا سوف يتيح لكم موقع المرجع فرصة التعرف على إجابة ما طُرِح من سؤالٍ غاية في الأهمية، إلى جانب بعض المواضيع المتعلقة به.
العناصر في الجدول الدوري تترتب حسب اعدادها الكتلية
ندفع إليكم الإجابة الأصحّ والأفضل للسّؤال الّذي قد ورد في كتاب علم الكيمياء لهذا الفصل الدّراسيّ، والذي ينصّ على “العناصر في الجدول الدوري تترتب حسب أعدادها الكتليّة ؟”، فإنّ الإجابة هي:
- عبارة خاطئة.
حيث أنّه تمّ ترتيب العناصر في الجدول الدوري تبعًا للعدد الذري وليس العدد الكُتلي، والذي يضم عدد البروتونات والنيوترونات المتواجدة في النواة، ولكن العدد الكتلي هو عدد وحيد يتواجد لكل نظير من العناصر، حيث يتم كتابته بعد اسم العنصر أو في أعلى يسار العنصر بحجمٍ صغير، وهكذا تمّ توضيح الإجابة الصحيحة للعبارة السابقة.
أهميّة الجدول الدوري
تكمن أهميّة الجدول الدوري في عدّة أمور متنوّعة تسهّل الوصول السريع من خلال خصائصه، وهي تتلخّص فيما يأتي:[1]
- معرفة سلوك العنصر الكيميائي.
- معرفة البنية الإلكترونيّة لذرات العناصر.
- تحديد موقع العنصر في الدورة أو المجموعة.
- التنبؤ بالتفاعلات الكيميائيّة التي يدخل فيها العنصر الكيميائي.
خصائص الجدول الدوري
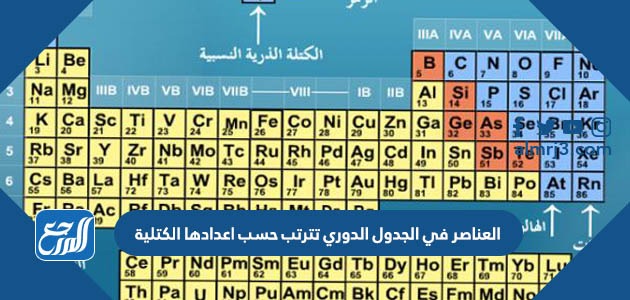
إنّ من أبرز خصائص الجدول الدوري والتي تتلخّص في الآتي، حيث أنّ الجدول الدوري رُتّبت عناصره الكيميائيّة في صفوف وأعمدة كما هو موضح في الصورة أعلاه، ومن خصائصه:
- يوجد به 118 عنصر كيميائي.
- معظم العناصر عبارة عن معادن قلوية، ترابيّة، انتقاليّة، معادن أساسيّة.
- يحتوي على سبع دورات أفقيّة.
- يحتوي على 18 أعمدة رأسيّة (مجموعة).
- يعتمد الجدول الدوري في تصنيف عناصرها على الزيادة في العدد الذري.
- عناصر المجموعة الواحدة متشابهة في نفس الخصائص ولها نفس الترتيب في المدار الأخير.
- عناصر المجموعة الأولى والثانية والثالثة تميل لفقد الإلكترونات.
- عناصر المجموعة الرابعة والخامسة والسادسة تميل لكسب الإلكترونات.
- كل دورة في الجدول الدوري تنتهي بعنصر خامل (نبيل)، مداره الأخير ممتلئ.
- إلكترونات المدار الأخير للعنصر أو إلكترونات التكافؤ، تحدد رقم الدورة التي ينتمي لها العنصر.
- أسفل الجدول الدوري هناك سلسلتان طويلتان من العناصر تسمى الأولى (لانثانيدات)، والثانية (أكتنيدات)، وكل منها تحتوي على 14 عنصر.
- تصنّف عناصر الجدول الدوري إلى فلزات ولا فلزات وبينهما أشباه فلزات.
وبهذا القدر من المعلومات نكون قد وصلنا وإياكم إلى نهاية فقرات هذا المقال المطروح، والذي كان بعنوان العناصر في الجدول الدوري تترتب حسب اعدادها الكتلية؟، بالإضافة إلى التعريف العام عن العناصر في الجدول الدوري.
المراجع
- thoughtco.com , Why Is the Periodic Table Important? , 19/12/2021
















