بحث عن العناصر الممثلة
جدول المحتويات
بحث عن العناصر الممثلة يعتبر العنصر بانها مادة تتكون من الذرات، كما لا يمكن تقسيمها لمواد أبسط باستخدام الطرق الكيميائية العادية، كما تتكون عناصر الجدول الدوري من ثماني مجموعات، حيث تكون إما عناصر انتقالية أو عناصر ممثلة، حيث تعتبر العناصر الممثلة بأنها العناصر الكيميائية التي تندرج فيها الخواص الكيميائية والفيزيائية بشكل تدريجي منتظم، ومن هذا المنطلق ومن خلال سطورنا التالية عبر موقع المرجع سيتم تقديم بحثًا شاملًا عن العناصر الممثلة وأهميتها.
مقدمة بحث عن العناصر الممثلة
يعتمد علم الكيمياء على تنظيم العناصر الكيميائية وفق جدولًا دوريًا، حيث أن كل عنصر من العناصر الكيمائية له صفات وخصائص تختلف عن غيره، فقد تم تقسيم الجدول إلى مجموعات لتصنيف العناصر، بحيث يتم وضع العناصر المشتركة بالخواص الكيميائية والفيزيائية مع بعصها، حيث تعتبر العناصر الممثلة أحد العناصر التي توجد في الجدول الدوري، كما ان لها أهمية كبيرة، بالإصافة إلى العديد من الاستخدامات، وفي هذا المقال سيتم بيان أبرز المعلومات عن العناصر الممثلة.
بحث عن العناصر الممثلة
يعتبر الجدول الدوري بأنه أحد أهم الإنجازات في العلوم، حيث قام العديد من العلماء بتنظيم العناصر لكن نشر ديمتري مندلييف النسخة الأولى من الجدول الدوري في عام 1869، حيث يُنسب إليه الجدول الدوري باعتباره مخترعه وأول من نظمه، فقد تطور الجدول الدوري ليوضح التطور العلمي في الكيمياء، حيث هناك 118 عنصرًا بحيث يتم تصنيفهم إلى عناصر ممثلة أو عناصر انتقالية، حيث تشمل العناصر الممثلة 8 مجموعات وكل مجموعة تحتوي على عدد من العناصر والتي يكون لها مجموعة من الخصائص، كما سيتم تقديم بحثًا شاملًا حول العناصر الممثلة في الجدول الدوري.
الجدول الدوري
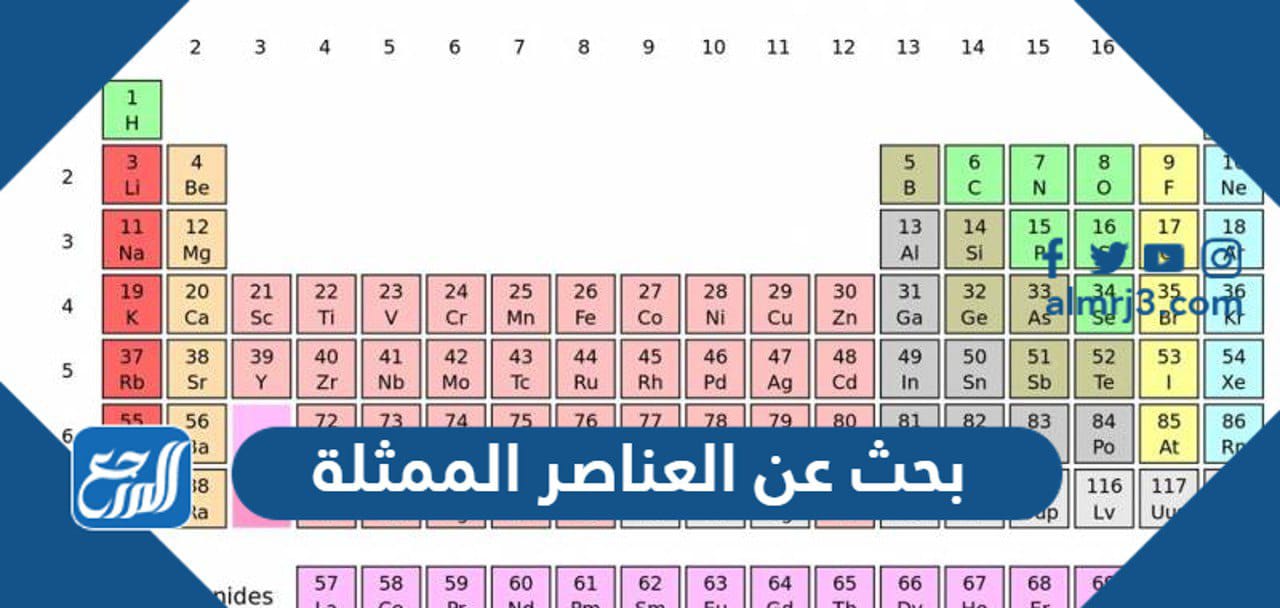
يعتبر الجدول الدوري بأنه الترتيب المنظم من 118 عنصرًا كيميائيًا، حيث يتم ترتيب هذه العناصر الكيميائية من اليسار إلى اليمين، وأيضًا من أعلى إلى أسفل بترتيب زيادة العدد الذري أو عدد البروتونات في نواة الذرة، فهي تتزامن بشكل عام مع زيادة الكتلة الذرية، إذ تسمى الصفوف الأفقية في الجدول الدوري بالدورات، حيث يشير رقم كل دورة إلى عدد المدارات للعناصر الموجودة في هذا الصف، أما العناصر التي توجد بنفس العمود في الجدول الدوري تسمى المجموعة لها تكوينات إلكترون تكافؤ متطابقة، كما هناك مفهومين من أحد المفاهيم المهمة في الجدول الدوري وهي كالآتي:[1][2]
- العدد الذري: وهو يبين عدد البروتونات في نواة الذرة.
- العدد الكتلي: وهو مجموع عدد البروتونات والنيوترونات.
شاهد أيضًا: الدوره في الجدول الدوري هي صف
مفهوم العناصر الممثلة
تعتبر العناصر الممثلة بأنها العناصر الكيميائية التي توجد في الجدول الدوري، فهي تجمع بين اللافلزات والفلزات، كما أن بعض العناصر الممثلة هي عبارة عن أشباه فلزات، حيث أن معظم المعادن الممثلة بشكل طبيعي تكون حالة غير مجمعة لأنها تتفاعل بسهولة مع الماء والأكسجين في الهواء، كما تعرف العناصر الممثلة بأنها من العناصر الأكثر وفرة على وجه الأرض، حيث تقسم العناصر الممثلة إلى 8 مجموعات وكل مجموعة تحتوي على عدة عناصر بينها مجموعة من الخواص الفيزيائية والكيميائية المشتركة وهي على النحو الآتي:[3]
عناصر المجموعة الأولى
تعتبر هذه العناصر بأنها معادن ناعمة ولامعة ومنخفضة الانصهار وعالية التفاعل، كما تتلطخ عند تعرضها للهواء، فقد تم تسميتها بالفلزات القلوية وفقًا لإذابة هذه المعادن أو أكاسيدها في الماء مما ينتج عنها محلول أساسي قلوي، حيث تعتبر بأنها نادرًا ما توجد في شكلها الأولي في الطبيعة، كما تحتوي الفلزات القلوية على إلكترون تكافؤ واحد فقط في مداراتها عالية الطاقة، فهي تكون كمركبات أيونية باستثناء الهيدروجين، حيث من أبرز هذه العناصر ما يلي:[4]
| اسم العنصر | رمز العنصر |
| الهيدروجين | H |
| الليثيوم | Li |
| الصوديوم | Na |
| البوتاسيوم | K |
| الروبيديوم | Rb |
| السيزيوم | Cs |
| الفرانسيوم | Fr |
شاهد أيضًا: تزداد حجوم ذرات عناصر المجموعة الواحدة كلما
عناصر المجموعة الثانية
تعتبر المجموعة الثانية من مجموعات الجدول الدوري بأنها تسمى الفلزات القلوية الأرضية، حيث لها العديد من الميزات فهي أكثر صلابة وأقل تفاعلًا من الفلزات القلوية، كما سميت بهذا الاسم بسبب أن أكاسيد هذه المعادن قامت بإنتاج محاليل أساسية عند إذابتها في الماء، فقد بقيت صلبة عند درجات الحرارة، وتحتوي على إلكترونين في غلافها الفرعي الخارجي، فهي تعتبر شديدة التفاعل بحيث لا يمكن العثور عليها في الطبيعة في شكلها الأولي، ومن هذه العناصر ما يلي:[5]
| اسم العنصر | رمز العنصر |
| البريليوم | Be |
| والمغنيسيوم | Mg |
| الكالسيوم | Ca |
| السترونشيوم | Sr |
| الباريوم | Ba |
| الراديوم | Ra |
شاهد أيضًا: تزداد طاقة التاين في الجدول الدوري لكل دورة
عناصر المجموعة الثالثة عشر
تعتبر المجموعة الثالثة عشر من مجموعات الجدول الدوري بأنها تسمى مجموعة البورون، حيث توجد ثلاثة إلكترونات في أجزاء الغلاف الخارجي لها، تتفاعل جميع عناصر المجموعة 13 عند درجة حرارة عالية مكونة ثلاثي أكسيد، تتفاعل مع الهالوجينات عند درجات حرارة عالية لتكوين ثلاثي هاليدات، يتحد البورون مع المعادن لتشكيل البوريدات، أما باقي عناصر المجموعة 13 لا تندمج مع المعادن، حيث تتكون هذه المجموعة من خمسة عناصر وهي كالآتي:[6]
| اسم العنصر | رمز العنصر |
| البورون | B |
| الألمنيوم | Al |
| الجاليوم | Ga |
| الإنديوم | In |
| الثاليوم | Tl |
عناصر المجموعة الرابعة عشر
تعتبر المجموعة الرابعة عشر من مجموعات الجدول الدوري بأنها تسمى مجموعة الكربون، تتكون المجموعة من الكربون وجميع العناصر التي توجد أسفله مباشرة في الجدول الدوري، حيث تقع في منتصف الجدول الدوري، كما توجد اللافلزات على يمينها والمعادن على يسارها، كما تحتوي على 4 إلكترونات في العلاف الخارجي لها، حيث تحتوي على معدن واحد غير معدني وهو الكربون، واثنين من أشباه الفلزات وهما السيليكون والجرمانيوم، ومعدنين وهما القصدير والرصاص، حيث تتكون عائلة الكربون من خمسة عناصر وهم:[7]
| اسم العنصر | رمز العنصر |
| الكربون | C |
| السيليكون | Si |
| الجيرمانيوم | Ge |
| القصدير | Sn |
| الرصاص | Pb |
تُعتبر المجموعة الخامسة عشر من مجموعات الجدول الدوري بأنها تسمى مجموعة النيتروجين، ويزداد حجم نصف القطر الذري أسفل المجموعة، كما أن تقارب الإلكترون يقلل من المجموعة، وتزيد نقطة الانصهار والغليان أسفل المجموعة، كما تتكون عناصر عائلة النيتروجين من ذرات تحتوي على 5 إلكترونات في غلافها الخارجي، حيث تكون العناصر صلبة في درجة حرارة الغرفة باستثناء النيتروجين، حيث تتكون عائلة النيتروجين من خمسة عناصر وهم:[8]
| اسم العنصر | رمز العنصر |
| النيتروجين | N |
| الفسفور | P |
| الزرنيخ | As |
| الأنتيمون | Sb |
| البزموث | Bi |
| المسكوفيوم | Mc |
شاهد أيضًا: أغلب العناصر الموجودة على يسار الجدول الدوري هي
عناصر المجموعة السادسة عشر
تعتبر المجموعة الخامسة عشر من مجموعات الجدول الدوري بأنها تسمى مجموعة الأكسجين، حيث يمكن العثور عليها في الطبيعة، فهي ترتبط ارتباطًا وثيقًا بالحياة، حيث يزداد نصف القطر الذري والأيوني مع انتقالنا من الأكسجين إلى البولونيوم، كما يعد الأكسجين والكبريت بأنهما لا يتبعوا للمعادن، أما السيلينيوم والتيلوريوم فهما أشباه فلزات، والبولونيوم معدنًا في ظل ظروف معينة وهو عنصر مشعًا، ويزداد الحجم الذري من الأكسجين إلى التيلوريوم، بالإضافة إلى ازدياد نقاط الانصهار والغليان، حيث تشمل عناصر المجموعة السادسة عشر ما يلي:[9]
| اسم العنصر | رمز العنصر |
| الأكسجين | O |
| الكبريت | S |
| السيلينيوم | Se |
| التيلوريوم | Te |
| البولونيوم | Po |
عناصر المجموعة السابعة عشر
تعتبر المجموعة الخامسة عشر من مجموعات الجدول الدوري بأنها تسمى مجموعة الهالوجينات، حيث أنها تقع على يسار الغازات النبيلة في الجدول الدوري، إذ أنها تشكل هذه العناصر المعدنية السامة، تعد عناصر الهالوجين بأنها تحتوي على سبعة إلكترونات تكافؤ في غلافها الخارجي، فإنها تتطلب إلكترونًا إضافيًا واحدًا فقط لتكوين ثماني إلكترونات لتصبح أكثر تفاعلًا من المجموعات غير المعدنية الأخرى، حيث تشمل عناصر المجموعة السابعة عشر ما يلي:[10]
| اسم العنصر | رمز العنصر |
| الفلور | F |
| الكلور | Cl |
| البروم | Br |
| اليود | I |
| الأستاتين | At |
| التينيسين | Ts |
شاهد أيضًا: تسمى الصفوف الأفقية في الجدول الدوري بالدورات
عناصر المجموعة الثامنة عشر
تعتبر المجموعة الخامسة عشر من مجموعات الجدول الدوري بأنها تسمى مجموعة الغازات النبيلة، حيث يتم ترتيبها وفقًا لدرجة غليانها، حيث يستخدم الزينون كمخدر بسبب قابليته العالية للذوبان في الدهون، كما يستخدم الرادون وهو شديد النشاط الإشعاعي ولا يتوفر إلا بكميات دقيقة في العلاج الإشعاعي، حيث أن نقاط الانصهار والغليان منخفضة للغاية، كما يُعتبر الغلاف الخارجي لإلكترونات التكافؤ بأنه ممتلئًا، ولها مجموعة من الخصائص حيث تعد غازات عديمة اللون والرائحة والطعم وهي غير قابلة للاشتعال إذ تعتبر الغازات النبيلة بأنها ستة عناصر وهي:[10]
| اسم العنصر | رمز العنصر |
| الهيليوم | He |
| النيون | Ne |
| الأرجون | Ar |
| الكريبتون | Kr |
| الزينون | Xe |
| الرادون | Rn |
خاتمة بحث عن العناصر الممثلة
يعتبر بحث العناصر الممثلة بأنه أحد البحوث العلمية المهمة فقد تناولنا وإيّاكم باقة مُتكاملة من الحديث حول مفهوم الجدول الدوري فهو يسهم في معرفة سلوك العناصر الكيميائية، وأيضًا معرفة البنية الإلكترونيّة لذرات العناصر، وقد أوضحنا في البحث مفهوم العناصر الممثلة، وانتقلنا في الحديث حول مجموعات العناصر الممثلة حيث أن المجموعة هي الأعمدة المكونة بشكل عمودي في الجدول الدوري فقد تم بيانها بالاستناد على عدد من المراجع العلمية، ونختم أخيرًا تدرج الصفات في الجدول الدوري وعلاقتها بالعناصر.
بحث عن العناصر الممثلة doc
تعتبر العناصر الممثلة هي من أحد العناصر التي توجد في الجدول الدوري، حيث لها أهمية كبيرة في حياة الإنسان، ولذلك نقدم هذا البحث كملف بصيغة doc يمكن تحميله “من هنا“، ليكون قابلاً للتحويل إلى ملف وورد متعدد الاستخدامات، كما يمكن طباعته على الورق ليكون مرجعاً أرشيفياً يمكن ضمه إلى المكتبة الشخصية.
بحث عن العناصر الممثلة pdf
إن العناصر الممثلة هي العناصر الكيميائية في الجدول الدوري التي تندرج الخواص الكيميائية والفيزيائية بشكل تدريجي منتظم، ونظراً لضرورة هذا البحث الذي أجريناه عن العناصر المملثلة وتصنيفها في الجدول الدوري وأبرز خواص كل مجموعة من مجموعاتها، كان لابد أن نقدمه كملف pdf يمكن تحميله “من هنا“، ليبقى مرجعًا يمكن العودة إليه وقت الحاجة.
شاهد أيضًا: تمكن موزلي من تطوير الجدول الدوري حسب الأعداد الكتلية
وبهذا القدر نصل إلى نهاية مقالنا الذي كان بعنوان بحث عن العناصر الممثلة، والذي خضنا من خلاله هذا البحث الهام عن العناصر الممثلة، بالإضافة إلى مجموعات العناصر التي تشتمل عليها العناصر الممثلة، كما تم تقديم هذا البحث كملف pdf وdoc لتحقيق الاستفادة منه.
المراجع
- acs.org , Periodic Table of Chemical Elements , 21/02/2022
- livescience.com , Periodic Table of Elements , 21/02/2022
- chem.libretexts.org , Periodicity - Chemistry LibreTexts , 21/02/2022
- thoughtco.com , Element Families of the Periodic Table , 21/02/2022
- chem.libretexts.org , Group 2: General Properties , 21/02/2022
- britannica.com , boron group element , 21/02/2022
- britannica.com , carbon group element , 21/02/2022
- britannica.com , nitrogen group element , 21/02/2022
- britannica.com , oxygen group element , 21/02/2022
- chem.libretexts.org , Group 17: The Halogens , 21/02/2022
- byjus.com , Group 18 Elements - Characteristics of Noble Gases , 21/02/2022





























