يتكون طيف الانبعاث الذري للهيدروجين من كم خط
جدول المحتويات
يتكون طيف الانبعاث الذري للهيدروجين من كم خط، إذ يعتبرُ طيف الانبعاث هو بصمةِ العنصر الذي يميزهُ عن غيره من العناصر المتواجدة في الطبيعة، وذلك عن طريق قياس أطوال خطوط الموجات الكهرومغناطيسية الصادرة عن قفزةِ الالكترون من مدارٍ لآخر، ومن خلالِ موقع المرجع سنوضحُ طيف الانبعاث لذرة الهيدروجين، وعدد خطوطِه.
طيف الانبعاث
طيف الانبعاث أو طيف الاصدار لعنصر ما هو عبارة عن الشدة النسبية للأمواج الكهرومغناطيسية الخاصة بكل تردد نتجَ عن انتقال الكترون ذرة العنصر من مدارٍ لآخر فيها نتيجةً للطاقة المكتسبة، وعندما يعودُ الالكترون الى مستوى الطاقة الذي انتقل منّه بفعل طاقتهِ المكتسبة فإنّ ذلك يكون على شكل شعاع ضوئي له تردد معين يُسمى الفوتون، وتحسبُ طاقة الفوتون عن طريقِ فرق الطاقة بين مداري انتقال الالكترون، ويوجدُ هنالك الكثيرَ من الانتقالات الالكترونية لكل ذرة مكونة للعنصر، والتي يكونُ لكلٍ منها فرق طاقة مختلف يؤدي الى انبعاث أطوال موجية مختلفة، ويتم استخدام مطياف الاصدار الذري في تحديد الأطوال.
يتكون طيف الانبعاث الذري للهيدروجين من كم خط
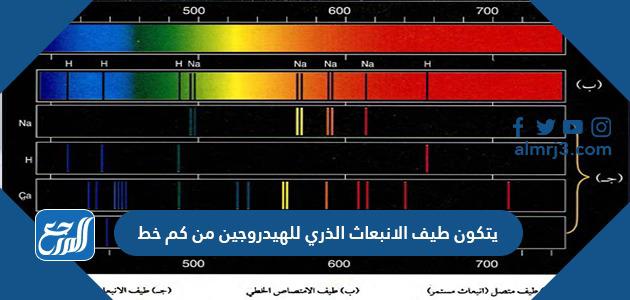
تنشأ خطوط طيف الانبعاث في ذرة الهيدروجين من انبعاث الفوتون الناتج عن انتقال الكترون الذرة بين مستوياتِ الطاقة المختلفة، وتكونُ اجابة سؤال يتكون طيف الانبعاث الذري للهيدروجين من كم خط، هي: [1]
- يتكونُ طيف الانبعاث الذري للهيدروجين من أربع خطوط موجية مختلفة الطول، حيثُ يتمُّ قياسها بالنانومتر، كما يتكونُ من بعض الخطوط الموجية في نطاقِ الأشعة الفوق بنفسجية.
وتتراوح أطوال الخطوط الموجية المرئية ألفا في طيفِ الانبعاث الذري للهيدروجين ما بين 400 – 600 نانومتر، في حين أن أطوال الخطوط الموجية الغير مرئية المتواجدة في نطاقِ الأشعة فوق البنفسجية تقلُّ عن 400 نانومتر.
خطوط طيف الهيدروجين
تنقسم خطوط طيف الهيدروجين إلى عدة مجموعاتٍ من الأطياف، والتي تكونُ مختلفة الأطوال، إذ تمّ قياسُ أطوالها بناءً على معادلةِ ريديرغ التي تصفُ الخطوط الطيفية في الفيزياءَ الذرية، ويتمّ تمثيل خطوط طيف الهيدروجين عن طريقِ نموذج بور، والذي يوضحُ انتقال الالكترون ما بين مستويات الطاقة المُختلفة بفعلِ الطاقة المكتسبة بواسطةِ التسخين أو أيّ عاملٍ آخر، وتتجمعُ خطوط الطيف في شكلِ مجموعات أو مسلسلات، بحيثُ تبدأ كل مجموعة بالخط ذو أطول موجة وأقل تردد، فالعلاقة عكسية ما بين الطول الموجي والتردد، وفي بعضِ الأحيان تختلطُ خطوط طيف الهيدروجين بخطوط أطياف عناصر أخرى مثل الهيليوم والهيدروجين، وذلك تحت تأثير الشمس وعند التحليل في الهواء.
طيف ذرة الهيدروجين pdf
تفسرُ ظهور خطوط طيف الهيدروجين اكتساب الذرة لطاقة خارجية مؤثرة، بحيثُ تعملُ على انتقال الالكترون من مداره الى مدار آخر يحددٌ بناءً على الطاقة المكتسبة، فكلما زادت الطاقة المكتسبة يصبحُ التباعد بين المستوياتِ أقل، وتمّ تفسيرُ ذلك بناءً على نموذج بور، والذي وضح بشكل مبسط طيف الانبعاث لذرة الهيدروجين، ويمكنُ قراءة المزيد من المعلوماتِ حول طيف ذرة الهيدروجين pdf “من هنا” .
الى هنا نكون قد وصلنا الى نهايةِ مقالنا يتكون طيف الانبعاث الذري للهيدروجين من كم خط، والذي يتكونُ من أربع خطوط مرئية، وخطوط غير مرئية في نطاقِ الأشعة فوق البنفسجية، كما سلطنا الضوء على خطوط طيف الهيدروجين ومصادرها.
المراجع
- libretexts.org , The Atomic Spectrum of Hydrogen , 04/09/2021